Дедалі більшої уваги набуває відносно нещодавно описаний феномен дистанційної взаємодії пухлини зі здоровими тканинами організму через секрецію екзосом. Деякі злоякісні клітини здатні до виділення у міжклітинний простір та тілесні рідини наноскопічні везикули – кулясті мішечкі, оточені плазматичною мембраною, які можуть містити різноманітні активні речовини, здатні впливати на фізіологічні процеси, що проходять всередині нормальних клітин. Вчені припускають, що таким чином трансформовані клітини можуть впливати на оточуючі тканини і програмувати їхню діяльність на підтримання пухлини. Зокрема у 2012 році вчені Університету Штату Огайо продемонстрували здатність пухлин пригнічувати імунну відповідь за допомогою екзосом, що містили мікроРНК. А нещодавнє дослідження вчених Техаського Університету виявило взагалі неймовірні речі: біогенез мікроРНК може автономно проходити у везикулах, а потрапляння їх вмісту в нормальні епітеліальні клітини може призводити до їхнього неопластичного переродження. Фактично, отримано ще один доказ того, що «рак» може передаватися від клітини до клітини.
Дедалі більшої уваги набуває відносно нещодавно описаний феномен дистанційної взаємодії пухлини зі здоровими тканинами організму через секрецію екзосом. Деякі злоякісні клітини здатні до виділення у міжклітинний простір та тілесні рідини наноскопічні везикули – кулясті мішечкі, оточені плазматичною мембраною, які можуть містити різноманітні активні речовини, здатні впливати на фізіологічні процеси, що проходять всередині нормальних клітин. Вчені припускають, що таким чином трансформовані клітини можуть впливати на оточуючі тканини і програмувати їхню діяльність на підтримання пухлини. Зокрема у 2012 році вчені Університету Штату Огайо продемонстрували здатність пухлин пригнічувати імунну відповідь за допомогою екзосом, що містили мікроРНК. А нещодавнє дослідження вчених Техаського Університету виявило взагалі неймовірні речі: біогенез мікроРНК може автономно проходити у везикулах, а потрапляння їх вмісту в нормальні епітеліальні клітини може призводити до їхнього неопластичного переродження. Фактично, отримано ще один доказ того, що «рак» може передаватися від клітини до клітини.
Екзосоми створюють імуно-толерантне пухлинне мікрооточення
Вивчення секреторних везикул злоякісних клітин почалося із ціллю пошуку нових надійних методів визначення біомаркерів раку. Оскільки екзосоми часто транспортуються із током тілесних рідин і містять пухлинні білки та РНК, вони являють легко доступний матеріал для діагностичного дослідження. Але біологи ні на крок не відставали від клініцистів, і провадили суто фундаментальні дослідження пухлинних екзосом. Так на початку нинішнього десятиліття стало відомо, що везикули порушують нормальний розвиток імунних клітин та негативно впливають на формування імунної відповіді проти пухлини. Зокрема такі ефекти опосередковані трансформуючим фактором β, асоційованим із зовнішньою мембраною екзосоми у зв’язаній із гепаран-сульфатом формі. Такий так званий латентний TGF-β може активно взаємодіяти із рецепторами Т-клітин і спрямовувати їхню диференціацію у регуляторні клітини, тим самими зменшуючи популяцію ефекторних клітин, пригнічуючи протипухлинну імунну відповідь. Іншим гальмуючим фактором може бути аденозин, який утворюється із міжклітинної АТФ під дією поверхневих ензимів екзосом, головно CD39 and CD73. Наявність аденозину в пухлинному мікрооточенні може пригнічувати низку ефекторних Т-клітин шляхом зв’язування із А2А рецептором цих клітин.

Будова злоякісної екзосоми. Вона несе характерні поверхневі маркери – білки родини тетраспанінів, а також інтегрини, що допомагають їй зливатися із мембранами цільових клітин. Внаслідок такого злиття відбувається вивільнення її вмісту в цитоплазму, а також інтеграція трансмембранних протеїнів до мембрани цільової клітини. Функції компонентів екзосоми розглядаються у тексті. Адаптовано з Clayton, A. Cancer cells use exosomes as tools to manipulate immunity and the microenvironment. OncoImmunology. Vol.1, No.1, (February, 2012): 78-80.
Феномен горизонтально перенесення онкогену екзосомами
Важливо розуміти, що злоякісні клітини не винаходять нічого нового, а лише використовують клітинні механізми, які є надбанням довгих років еволюції і взагалі-то мають слугувати на благо організму. Так само виходить і з мікровезикулярним транспортом, який є важливою складовою міжклітинної комунікації, таким самим за значенням, як і порівняно краще вивчений на сьогоднішній день обмін сигнальними молекулами (цитокінами, хемокінами, факторами росту, про-апоптотичними лігандами, тощо.) Виявляється, що клітини раку є експертами зі спотворення нормального функціонування оточуючих клітин за допомогою екзосом. Відтак у 2008 році в респектабельному журналі Nature Cell Biology було опубліковане дослідження вчених Університету МакГілл, де вони продемонстрували, що клітини злоякісної гліоми можуть розповсюджувати мутантну форму рецептору епідермального фактору росту EGFRvIII. І роблять вони це за допомогою вбудовування видозміненого варіанту EGFR в мембрану екзосоми, яка потім зливається із мембраною іншої клітини гліоми. EGFRvIII призводить до активації основні сигнальні шляхи проліферації та виживання клітини (через обидва шляхи PI3K/Akt та MAPK), а також підвищує здатність до інвазивного росту. Якщо трансформована клітина ще не набула потрібної мутації і не експресує на поверхні EGFRvIII, то вона має змогу отримати його «в подарунок» від сусідньої злоякісної клітини, і таким чином загальний рівень злоякісності пухлини зростає. Це являє собою абсолютно новий феномен, у якому задіяні екзосоми. Передача онкогенного протеїну від клітини до клітини отримала назву «горизонтальне перенесення онкогену» і є однією зі складових так званого ефекту онкогенного поля (oncogenic “field effect”), та про це якось іншим разом. Пізніше у 2012 році інша міжнародна дослідницька група представила ще один приклад переносу онкогенного рецептору злоякісними екзосомами. Вони показали, що вони на пряму задіяні в утворенні так званих метастатичних ніш у низці органів пацієнта, тобто забезпечують сприятливі умови для метастазування пухлини. Мікровезикули, які клітини випускають злоякісної меланоми у систему кровообігу пацієнта, взаємодіють там із нечисленною популяцією клітин – ранніми попередниками гемопоезу (bone marrow derived progenitor cells). Внаслідок такої взаємодії клітина-попередник отримує від екзосоми фосфорильований, тобто вже активований, рецептор MET. Таке «придбання» змінює транскрипційну програму клітин-попередників, і вони ініціюють неоангіогенез навколо пухлини, а також підтримують ендотелій судин у релаксованому стані, що полегшує екстра- та інтравазацію клітин метастазуючої пухлини. Важливим висновком з проведеного дослідження стало те, що екзосоми, ізольовані з крові, можна використовувати для встановлення метастатичного статусу пухлини, а також те, що ген Rab27a меланоми є ключовим у процесі секреції мікровезикул, а відтак – може розглядатися як терапевтична ціль для пригнічення метастазування зазначеного злоякісного новоутворення.

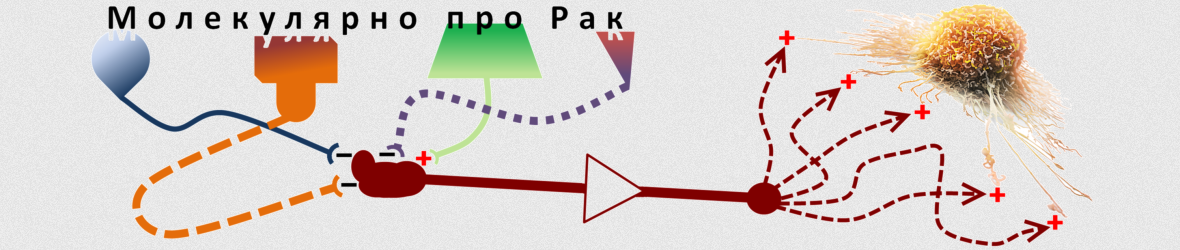
Механізм горизонтального перенесення онкогену. Зліва показана злоякісна клітина, що несе мутацію, яка уможливлює експресію онкогенного рецептору. Через порушення сигналювання в такій клітині, рецептор зазвичай є вже активованим (фосфорильованим) на час пакування у екзосому. Шляхом екзосомального транспорту такий рецептор потрапляє до клітини, яка ще не набула мутації, потрібної для власної продукції онкогену (показана справа). Поява рецептору може змінювати сигнальні каскади всередині клітини-реципієнта.
Екзосоми містять дволанцюгові мікроРНК, які запускають хронічне запалення
За останні два роки у центр уваги досліджень пухлинних екзосом з’явилися РНК молекули, які містяться у них. В них можуть міститися абсолютно різноманітні типи РНК: мРНК, тРНК а також малі інтерферуючі РНК також знані як мікроРНК. Останні являють собою короткі олігорибонуклеотиди від 19 до 24 основ і викликають найбільше інтересу дослідників ракових екзосом, оскільки вони володіють потенційною можливістю пригнічувати експресію певних генів. В цьому контексті окремої уваги заслуговують miRNA-21 та miRNA-29. Відтак, дослідники Університету Штату Огайо у 2012 році чітко визначили, що вони беруть участь у прогресії та метастазуванні пухлин, щоправда, трохи у незвичайний спосіб. Екзосоми, що вивільняються клітинами раку легенів (in vitro) здатні доставляти згадані вище мікроРНК всередину інших клітин. Але надалі ці РНК молекули не пригнічують експресію цільових генів як зазвичай, а натомість, взаємодіючи зі спеціальними внутрішньоклітинними рецепторами клітин-реципієнтів, викликають хронічне запалення навколо пухлини, що є однією з передумов її метастазування. Мова йде про зв’язування мікроРНК із Toll-like рецепторами, зокрема TLR8, який саме відповідає за розпізнавання одноланцюгових РНК фрагментів довжиною не більше 20-ти нуклеотидів. Методами флуоресцентної мікроскопії вчені продемонстрували колокалізацію miRNA-21, miRNA-29 з ракових екзосом та TLR8 всередині реципієнтної клітини, а потім підтвердили факт зв’язування цих мікроРНК із рецептором шляхом імунопреципітації TLR8 із наступним проведення кількісної ПЛР в реальну часі (quantitative real-time PCR) для визначення відповідних мікроРНК. Надалі зі застосуванням нокаутних ліній мишей та маніпуляцій із лейкоцитами людини in vitro, дослідники визначили, що активація TLR8 зазначеними мікроРНК веде до NF-κB-опосередкованого зростання продукції цитокінів запалення TNF-α та IL-6. Як відомо, хронічне запалення як системне так і в місці локалізації пухлини є ознакою просунутої стадії пухлинної хвороби і одним з факторів, що сприяє уникненню імунної відповіді та метастазуванню раку.

Запуск програми хронічного запалення екзосомальними мікроРНК. miRNA-21 та miRNA-29, які містяться у злоякісних екзосомах, можуть потрапляти в ендосоми всередині клітини-реципієнта, де надалі зв’язуються із Toll-like рецептором 8. Його активація веде до старту експресії про-інфламаторних цитокінів. Оскільки цей процес відбувається постійно, навколо пухлини проходить хронічний запальний процес, результатом якого стає пригнічення протипухлинного імунітету та метастазування раку.
Екзосомальні мікроРНК, які можуть впливати на транскриптом цільових клітин і викликати їх злоякісне переродження
Інше дослідження Техаського Університету, опубліковане на днях, показує, що мікроРНК злоякісних екзосом раку молочної залози усе-таки здатні напряму впливати на експресію генів в оточуючих пухлину нормальних тканинах. Більше того вони за допомогою флуоресцентних та імунологічних методів встановили, що до складу екзосом окрім власне мікроРНК входять також усі білки так званого RNA induced silencing complex (RISC): Diser, AGO2 та TRBP. Ці протеїни необхідні для перетворення попередників мікроРНК (пре-мікроРНК) на активні молекули, здатні спричиняти сайленсінг генів. Методом коімунопреципітації було виявлено факт збірки активного RISC-комплексу в екщосомах, а за допомогою норзен блоту вчені змогли спостерігати конверсію пре-мікроРНК у активні мікроРНК. Це є першою демонстрацією того факту, що біогенез мікроРНК може проходити поза клітиною – автономно у екзосомах. Дуже елегантним виглядає пояснення, чому злоякісні клітини не відправляють «голі» мікроРНК. Справа в тому, що самі по собі мікроРНК не є ефективними у пригніченні експресії генів, і можуть реалізовувати свою активність лише у випадку, якщо вони присутні в клітині у великій кількості (зазвичай, це досягається тільки в штучних контрольованих експериментальних умовах). Причиною цього є те, що вірогідність самочинного потрапляння мікроРНК до комплексу RISC є досить малою. Тому починаючи від транскрипції пре-мікроРНК і до утворення активного комплексу RISC-мікроРНК , ця молекула повинна наче на конвеєрі передаватися від протеїну до протеїну для успішного виконання своєї задачі. Тож, шляхом утворення екзосом, в яких присутні всі необхідні елементи сайленсігу цільового гену, злоякісна клітина забезпечує вищу вірогідність досягнення своєї мети – зміни поведінки оточуючих нормальних тканин.
Потрапляння усіх компонентів дистанційного пригнічення трансляції генів до екзосоми залежить від функціонування CD43 – трансмембранного сіалоглікопротеїну. Нещодавно було висловлено припущення щодо ймовірної ролі CD43 в утворенні екзосом. У даному досліджені було виявлено факт взаємодії протеїну Dicer та CD43. Також було помічено, що у разі нокдауну CD43 відбувається різке скорочення кількості протеїну Dicer у екзосомах і зростання – у цитоплазмі клітин раку. Збільшення рівня експресії CD43 є характерним для низки солідних пухлин, включно із раком молочної залози, тоді як у нормальних епітеліальних клітинах його продукція є стабільно низькою. Враховуючи виключну роль цього сіаломуцину в утворення злоякісних екзосом і його кореляцію із прогресією та метастазуванням пухлин, CD43 можна розглядати як ціль для таргетної терапії, наприклад, із використанням моноклональних антитіл.
Далі – більше. мікроРНК та Dicer, що транспортуються екзосомами, можуть викликати злоякісне переродження епітеліальних клітин. Було встановлено, що у разі культивування лінії клітин нормальних епітеліоцитів молочної залози із екзосомами, отриманими від злоякісних клітин, спостерігається зміна експресії 108 генів. Зокрема було відмічено зниження експресії генів PTEN та HOXD10 під дією екзосомальних мікроРНК miRNA-21 та miRNA-10b, відповідно. Перший ген є супресором пухлинного росту, а другий відповідає за правильну диференціацію епітеліоцитів. Вчені припускають, що порушення їхньої активності може призводити до набуття клітинами злоякісного фенотипу: підвищеної здатності до проліферації та відсутності диференціювання у зрілі епітеліоцити. Важливим спостереженням є те, що такий ефект екзосомальних мікроРНК повністю залежав від активності протеїну Dicer у них, оскільки у разі блокування цього білка (за допомогою введення до екзосом Dicer-специфічного антитіла шляхом електропорації) сайленсінгу цільових генів не відбувалося. Подібно до цього результату, отриманого in vitro, реалізувати онкогенний потенціал на моделі мишачої карциноми in vivo могли лише екзосоми із незаблокованим Dicer. Надалі вчені проаналізували склад сироватки крові різних пацієнтів, хворих на рак молочної залози, рак ендометрію та рак яєчника, і виявили у них точнісінько ті самі екзосоми, що містили мікроРНК, усі протеїну RISC комплексу, і також були здатні до перетворення пре-мікроРНК в активні форми. Екзосоми, отримані від пацієнтів, також підтвердили свою здатність до утворення пухлин в мишах in vivo. Тож, цілком можливо, що усі описані вище ефекти притаманні не лише експериментальним системам, а й реальним пухлинам. Як висловився керівник дослідницької групи Raghu Kalluri: «Уявіть це собі, як дитина дме на стиглу кульбабку і вітер несе її насіння на свіже покошену галявину, тоді ви зрозумієте, як цей молекулярний міксер розносить захворювання по оточуючих тканинах».

Дистанційна репресія генів клітиною раку. Злоякісні клітини можуть доставляти активні комплекси РНК-індукованого сайленсінгу генів, спрямованого проти конкретних мРНК молекул. Варто відзначити, що біогенез мікроРНК відбувається безпосередньо в екзосомах, що забезпечує вищу вірогідність нокдауну цільового гену в клітині-реципієнті.
Цікавим спостереженням є те, що збільшення кількості мікроРНК у пухлинних екзосомах не є наслідком зростання експресії мікроРНК у окремих злоякісних клітинах загалом – у цитоплазматичній фракції таких клітин концентрація цих молекул є порівняно невеликою. А на фоні того, що мікроРНК пакуються в екзосоми разом із ензимами RISC комплексу, виходить що, у клітини раку працює спеціальна генетична програма з вироблення і доставки активних мікроРНК до нормальних клітин. Таким чином, можемо бачити, що клітини пухлини можуть маніпулювати оточуючими здоровими тканинами за допомогою системи екзосомального транспорту. Одним з ефектів екзосом є створення імуносупресорного та метастатичного пухлинного мікрооточення. Але особливо приголомшливим в цьому плані є принципова можливість горизонтально перенесення «злоякісності» від клітини до клітини будь то шляхом передачі онкогенного рецептора або за допомогою доставки активованих мікроРНК. Загалом, феномен горизонтального перенесення онкогенів додає новий рівень складності у наше і без того сплутане розуміння процесів розвитку пухлини, клональної еволюції та взаємодії пухлина-організм. Але лише подібні дослідження, що відкривають нові горизонти, можуть принести справжнє задоволення науковцю!
Посилання
Clayton, A. Cancer cells use exosomes as tools to manipulate immunity and the microenvironment. OncoImmunology. Vol.1, No.1, (February, 2012): 78-80.
Al-Nedawi K., Meehan B., Micallef J., et. al. Intercellular transfer of the oncogenic receptor EGFRvIII by microvesicles derived from tumour cells. Nature Cell Biology. Vol. 10, No. 5, (May, 2008): 619-624.
Peinado H., Alečković M., Lavotshkin S., et. al. Melanoma exosomes educate bone marrow progenitor cells toward a pro-metastatic phenotype through MET. Nature Medicine. Vol. 18, No. 6, (June, 2012): 883-891.
Fabbri M., Paone A., Calore F., et. al. MicroRNAs bind to Toll-like receptors to induce prometastatic inflammatory response. Proceedings of the National Academy of Science. Vol. 109, No. 31, (July, 2012): E2110-6.
Melo S.A., Sugimoto H., O’Connell J.T., et. al. Cancer Exosomes Perform Cell-Independent MicroRNA Biogenesis and Promote Tumorigenesis. Cancer Cell. Vol. 26, (November, 2014): 1–15.